고정 헤더 영역
상세 컨텐츠
본문

안녕하세요. 텔로머라제의 모든 것을 알려드리는 텔로머라제 홍보대사입니다.
텔로미어란?
염색체 끝 부분에 붙어있는 반복 염기서열로,
염색체의 손상을 막아주는 역할을 함
텔로머라제란?
텔로미어가 손상되면 복구, 생성해주는 효소
노화를 방지하는 효소
이번 포스트에서는 텔로머라제(Telomerase)가 사람의 기억력, 그 중에서도 공간기억(Spatial memory)에 끼치는 영향에 대해 알아보겠습니다.

공간기억(Spatial memory)이란, 특정 공간을 인식하고 기억하는 능력입니다. 쉽게 이해할 수 있도록 예를 들면, 다람쥐가 도토리를 숨겨놓은 장소를 나중에 가서도 찾을 수 있는 것이 이 공간기억을 갖고 있기 때문인데요.
사람의 해마(Hippocampus)에 있는 뉴런들이 이런 공간기억 형성에 관여한다고 알려져 있습니다. 해마에 있는 두 종류의 뉴런, 장소 뉴런(Place neuron)과 그리드 뉴런(Grid neuron)이 공간과 거리를 3차원적으로 특별하게 인식하게 만들고 기억으로 저장하는 역할을 하는 것이죠.
이번 블로그에서는 텔로머라제(Telomerase)가 해마 속의 뉴런을 조절해 공간기억에 영향을 끼친다는 논문이 있어 소개해드리려 합니다. 이 논문을 살펴보기에 앞서서 텔로머라제가 무엇인지 간단하게 설명드려야 논문 이해에 도움이 될 것 같은데요.

텔로머라제(Telomerase)는 염색체 속에 위치한 DNA의 끝부분, '텔로미어(Telomere)'를 보호해주는 효소입니다.
우리는 생명을 유지하기 위해 살면서 세포분열을 계속해서 진행합니다. 세포분열이 진행될 때마다 DNA 끝부분, 즉 텔로미어는 손상되며 점점 짧아지는데요. 계속 짧아지다가 세포가 더 이상 분열할 수 없을정도로 짧아지면, 세포분열을 더 이상 진행하지 못하고 노화가 시작되는 것이죠.
텔로머라제는 이 텔로미어의 길이를 유지, 보완해줌으로써 노화가 진행되는 것을 막아주는 것입니다. 그런데 이 논문에서는 텔로머라제가 텔로미어 길이를 유지해 노화를 막는 것 뿐 아니라, 우리의 기억력에도 영향을 끼친다는 것인데요.
이 논문에서는 텔로머라제 발현을 막은 쥐모델에서 공간 기억이 떨어진 것을 먼저 확인하고, 텔로머라제가 공간기억 형성에 끼치는 영향에 대해 자세히 다뤘습니다. 지금부터 그 내용을 자세히 알아보겠습니다.
● TERT -/-(텔로머라제 발현 억제) 쥐 모델의 공간기억

우선 텔로머라제의 구성에 대해 설명드려야 논문 이해가 수월할 것 같은데요. 텔로머라제는 RNA와 catalytic subunit(쉽게 말하면 효소부위)으로 이뤄져있습니다.
텔로머라제를 이루는 RNA를 TERC라고 하며, 효소부위를 TERT라고 합니다. TERT는 Telomerase reverse transcriptase의 약자로, 텔로머라제 역전사효소를 뜻합니다. 텔로머라제 작용 기전에서 이 내용에 대해 자세히 다뤘으니, 맨 아래 링크에서 한 번 보시는 것을 추천드립니다.
이 논문에서는 위에서 언급한 텔로머라제의 효소부위인 TERT 발현을 억제한 쥐모델로 실험을 진행했습니다. 이제부터 TERT 발현 억제 모델을 TERT-/-라고 명시하겠습니다.

이 TERT-/- 쥐들의 공간기억력을 측정하기 위해 Morris water maze(MWM) test를 진행했습니다. MWM실험은 설치류의 공간 기억력을 측정하는데 쓰이는 보편적 방법이라고 하는데요.



(A) 그래프는 TERT-/- 쥐의 공간기억력과 인지 기능이 WT(Wild-Type, 일반 쥐) 보다 낮음을 보여줍니다.
(E)그래프는 앞의 설명과 마찬가지로 WT의 공간기억력이 TERT-/- 쥐 보다 좋다는 것을 보여줍니다. 또한 TERT-/- 쥐 중 TERT를 주입한 쥐가 그렇지 않은 TERT-/- 쥐보다 공간기억력이 더 좋다는 것을 보여줍니다.
(H)그래프는 LV-TERT-shRNA-GFP라는 TERT발현 억제제를 넣은 쥐가 그렇지 않은 쥐보다 공간기억력이 더 낮은 것을 보여줍니다.
위 3개 그래프 결과로 TERT가 해마(Hippocampus)의 공간기억력과 기억형성에 큰 역할을 한다는 것을 알 수 있는 것이죠.
● TERT 주입 -> 공간기억력 향상

위 그래프에서 AD-GFP, AD-TERT-GFP가 무엇인지 궁금하실텐데요. 쉽게 생각해서 AD-TERT-GFP는 TERT를 주입한 모델이라고 생각하시면 되고, AD-GFP는 TERT를 주입하지 않은 모델이라고 생각하시면 됩니다.
(A)그래프는 AD-TERT-GFP 혹은 AD-GFP 주입 후 30일 뒤에 MWM test를 진행한 것이고, (B) 그래프는 주입 후 7일뒤에 MWM test를 진행한 것입니다. 앞에 내용에서 이미 언급해 예상하셨겠지만, 당연히 TERT를 주입한 모델에서 공간기억력이 더 좋다는 결과가 나왔습니다.
하지만 한 가지 신기한 점이 있는데요. 주입 7일뒤에 MWM test를 진행해 공간기억력을 비교한 것보다, 주입 30일 뒤에 MWM test를 진행한 모델에서 더 차이가 크게 나왔습니다. 즉, TERT 주입 7일 뒤 보다 30일 뒤 쥐들의 공간기억력이 더 좋다는 것인데요.
이 결과는 TERT가 공간기억력을 간접, 지연적(indirect, delayed)으로 향상시킨다는 것을 보여줍니다.
● TERT -/- 모델 -> 뉴런의 형태학적 변화 유발


(B)와 (C)의 뉴런 사진을 보면, TERT-/- 모델에서 뉴런의 수상돌기 길이와 branch 수가 WT보다 적다는 것을 알 수 있습니다. 이는 시각적으로 뿐 아니라 직접 길이를 재본 결과에서도 통계적으로 유의하게(P<0.05) 줄어들었다는 것을 알 수 있는데요.

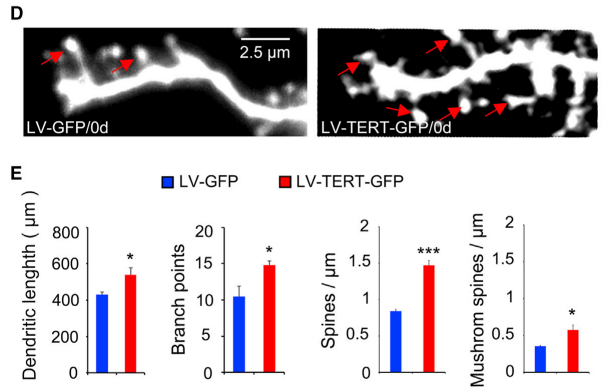
또한, TERT를 주입한 쥐 모델이 TERT를 주입하지 않은 쥐모델에서 보다 dendritic length와 synapsin 1 (신경전달물질 방출, 전달인자) 신호가 더 높다는 것을 알 수 있습니다. 또한, (D)사진을 보면 화살표 표시가 dendritic branch 수를 의미하는데요. 이 역시 TERT 주입 모델이 더 많은 것을 알 수 있습니다.
즉, TERT가 뉴런의 형태학(morphology)에 영향을 끼치고, 이로 인해 공간기억에 영향을 끼친다는 것을 알 수 있습니다.
● 마무리
이번 포스트에서는 TERT가 기억력에 어떤 영향을 끼치는지 알아보았습니다. 정확히 말하자면, 텔로머라제 발현이 우리의 기억력 중 공간기억에 어떤 영향을 끼치는지 알아봤는데요.
이 연구 뿐 아니라 최근 연구들에서는 텔로머라제 발현 억제가 우리의 뇌기능에 영향을 끼친다는 보고가 많이 되고 있습니다. 이번 실험에서는 텔로머라제 발현을 억제하기 위해 TERT-/- 쥐 모델을 사용했는데요. TERT 억제가 공간 기억력 저하에 영향을 끼친다는 것을 확인할 수 있었습니다.
해마 기능 장애는 기억력 장애, 더 악화되면 알츠하이머 치매와도 연관되어 있다고 하는데요. 텔로머라제가 공간기억 향상에 도움이 된다면, 알츠하이머 치매도 치료할 수 있는 가능성이 있는 것 아닐까요?
앞으로 텔로머라제 관련 논문들을 꾸준히 포스트 할 것인데요. 블로그에 자주 들러 관련 논문 내용을 많이 알아가셨으면 좋겠습니다.
글 마지막 부분에 관련 논문 보실 수 있게 링크 걸어두었으니 더 관심있으시면 한번 보시는 것을 추천드립니다.
*논문 출처
논문 제목 : Zhou, Q.-G., Liu, M.-Y., Lee, H.-W., Ishikawa, F., Devkota, S., Shen, X.-R., Jin, X., Wu, H.-Y., Liu, Z., Liu, X., Jin, X., Zhou, H.-H., Ro, E. J., Zhang, J., Zhang, Y., Lin, Y.-H., Suh, H., & Zhu, D.-Y. (2017). Hippocampal tert regulates spatial memory formation through modulation of Neural Development. Stem Cell Reports, 9(2), 543–556. https://doi.org/10.1016/j.stemcr.2017.06.014

'텔로미어, 텔로머라제 > 의학' 카테고리의 다른 글
| 퇴행성 관절염 치료 신약 후보 물질!! (0) | 2022.11.14 |
|---|---|
| 자폐증 치료 신약 후보 물질!!?? (0) | 2022.11.14 |
| '텔로머라제', 우울증과 공격성 완화!! (1) | 2022.11.14 |
| 텔로머라제, 뇌 기능에 끼치는 영향 (0) | 2022.11.11 |
| 텔로머라제와 텔로미어, 질병 바이오마커 역할!!?? (0) | 2022.11.10 |




